Elektrophile Reaktivität zur Bereitstellung bestimmter helikaler chiraler Gold(III)-Katalysatoren für die asymmetrische Synthese bioaktiver Verbindungen
Hanock Baiju – Hector RCD Awardee Agnieszka Nowak-Król
Hector Fellow A. Stephen K. Hashmi
Ziel des Projekts unter der Leitung von Hector RCD-Preisträgerin Agnieszka Nowak-Król (Universität Würzburg) und Hector Fellow A. Stephen K. Hashmi (Universität Heidelberg) ist die Entwicklung genau definierter helikaler chiraler Gold(III)-Komplexe – die ersten Beispiele für helikale chirale Goldkomplexe mit Goldatomen, die sich entweder am äußeren oder inneren Rand eines helikalen Systems befinden. Das katalytische Potential dieser neuartigen Komplexe und ihre praktische Anwendbarkeit sollen in der enantioselektiven Synthese von kleinen organischen Molekülen und biologisch oder pharmazeutisch relevanten Zielstrukturen, d.h. Naturstoffen und pharmazeutisch aktiven Verbindungen, demonstriert werden.
Chiralität spielt eine entscheidende Rolle in den Lebenswissenschaften und im Arzneimitteldesign. Der Begriff Chiralität bezeichnet die Eigenschaft eines Moleküls, in zwei unterschiedlichen, nicht zur Deckung bringbaren Formen zu existieren, die spiegelbildlich zueinander sind, wobei die atomare Zusammensetzung, die Atom-Atom-Verknüpfungen und die Bindungsordnungen unverändert bleiben. Da Enzyme und Rezeptoren in lebenden Organismen ebenfalls chiral sind, können sie unterschiedlich mit beiden Enantiomeren interagieren – also mit Stereoisomeren, die sich in der Konfiguration aller stereogenen Elemente unterscheiden. Aufgrund der unterschiedlichen räumlichen Anordnung der Atome im Molekül kann ein Enantiomer stärker und spezifischer an biologische Zielstrukturen binden als das andere. Diese spezifischen Wechselwirkungen bestimmen die Pharmakodynamik, Pharmakokinetik und Toxizität eines Wirkstoffs. Daher kann eine Form die gewünschte therapeutische Wirkung entfalten, während die andere inaktiv bleibt, eine geringere Wirksamkeit zeigt oder unerwünschte Nebenwirkungen verursacht.
Die Errungenschaften der Goldkatalyse in den letzten Jahrzehnten haben ihren festen Platz in der organischen Chemie etabliert. Im Allgemeinen arbeiten Goldkatalysatoren unter milderen Bedingungen effizienter als andere Übergangsmetallkatalysatoren, einschließlich niedrigerer Temperaturen, was den Abbau empfindlicher Substrate verhindern kann. Dies ist besonders vorteilhaft in der pharmazeutischen Synthese, wo die Erhaltung der strukturellen Integrität von entscheidender Bedeutung ist. Darüber hinaus bieten goldkatalysierte Umwandlungen eine hohe Atomeffizienz und Toleranz gegenüber funktionellen Gruppen und können eine orthogonale Reaktivität im Vergleich zu anderen Übergangsmetallkatalysatoren aufweisen.
Das Ziel dieses Projekts ist die Entwicklung einer neuen Klasse von Gold(III)-Komplexen, die von helikal-chiralen Chelatliganden abgeleitet sind und als Katalysatoren in goldvermittelten asymmetrischen Transformationen fungieren. Das Gold wird in das helikale Gerüst eingebaut, wobei derartige Komplexe bislang noch nicht bekannt sind. Die Helicenstruktur wird eine genau definierte, rigide chirale Umgebung um das Gold(III)-Zentrum schaffen und eine chirale Tasche formen, die selektiv mit prochiralen Substraten interagieren kann. Wir erwarten, dass dies eine hohe Enantioselektivität in gold(III)-vermittelten Reaktionen ermöglicht. Darüber hinaus kann das π‑konjugierte Gerüst eines gezielt designten Aurahelicens durch nicht-kovalente Wechselwirkungen die stereoselektiven Interaktionen mit einem Substrat verstärken, was zu einer hohen chiralinduzierten Steuerung führt. Diese Wechselwirkungen können weiter optimiert werden, indem die elektronischen Eigenschaften des Helicens durch die Einbindung ausgewählter Heterozyklen in das helikale Rückgrat oder durch gezielte Funktionalisierung mit elektronenziehenden oder elektronenabgebenden Gruppen modifiziert werden.
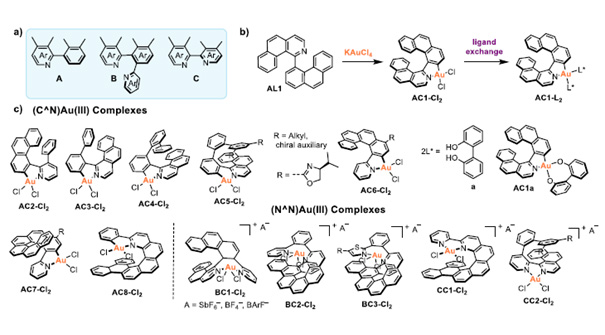
Figure: a) General motifs present in the target C^N and N^N ligands. Ar = six- or five-membered ring. b) Synthesis of a (C^N)Au(III) complex. c) Structures of selected target compounds.
Betreut durch

Agnieszka Nowak-Król
Chemie

A. Stephen K. Hashmi
ChemieHector Fellow seit 2010