Modellierung der extrazellulären Matrix des menschlichen erwachsenen Gehirns nach einer Verletzung zum Ziel der Reparatur
Meriam Ernez – Hector RCD Magdalena Götz
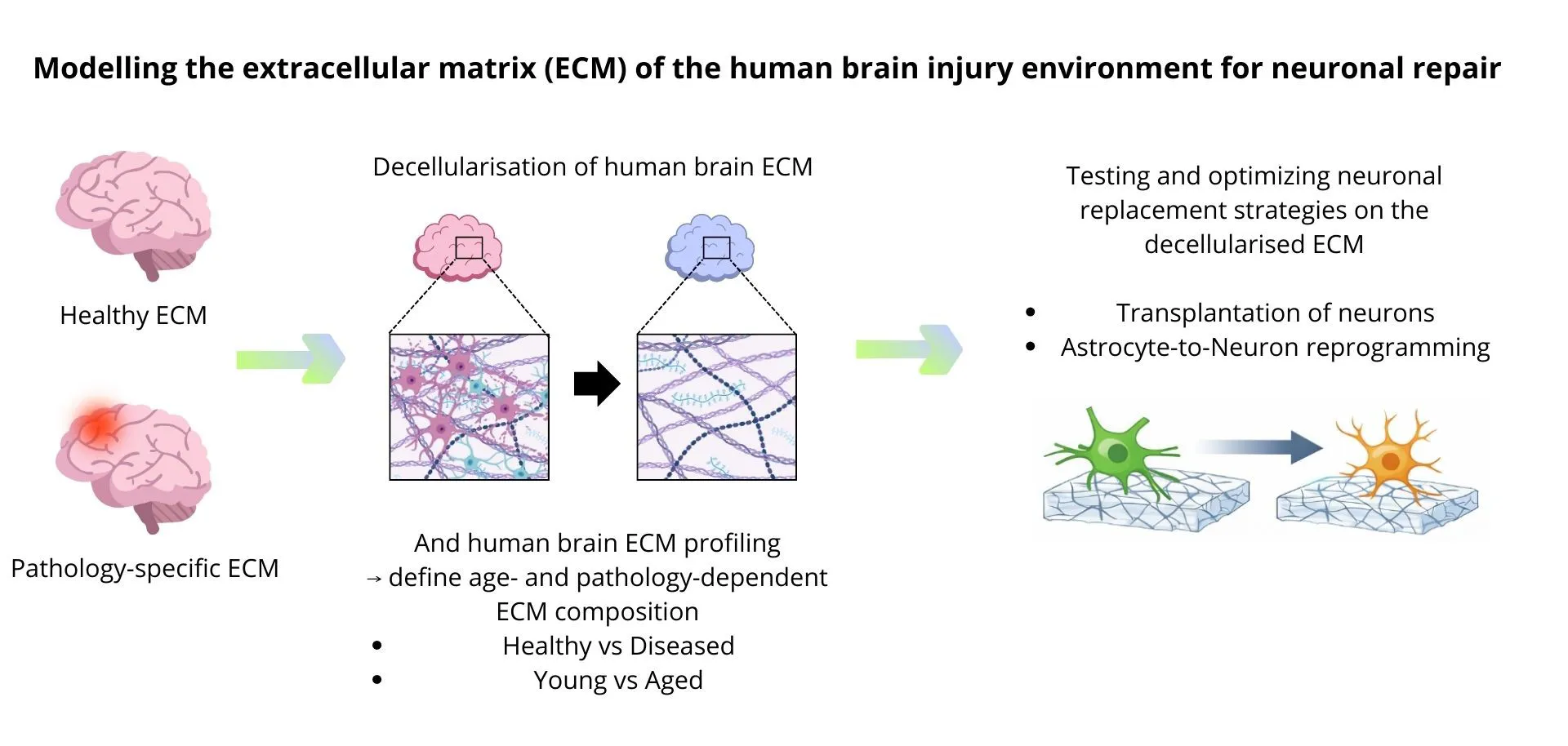
Hirnverletzungen und Neurodegeneration führen zu irreversiblem Neuronenverlust. Dieses Projekt modelliert die Verletzungsumgebung des erwachsenen menschlichen Gehirns durch Dezellularisierung von Hirngewebe adulter Patienten und Charakterisierung der extrazellulären Matrix (ECM). Strategien, abgestorbene Neurone zu ersetzen, einschließlich der Transplantation humaner iPSC-abgeleiteter Neuronen sowie der Reprogrammierung von iPSC-abgeleiteten oder aus Resektionsmaterial isolierten adulten Astrozyten, werden untersucht, um Bedingungen zu definieren, die neuronalen Ersatz über verschiedene Erkrankungen und Altersstufen hinweg ermöglichen.
Neuronaler Verlust tritt durch Alterung, neurodegenerative Erkrankungen oder Schlaganfall auf und ist beim Menschen weitgehend irreversibel. Die Regeneration im adulten menschlichen Gehirn ist stark begrenzt. Obwohl neuronale Transplantation und direkte Glia-zu-Neuron-Reprogrammierung vielversprechende Strategien darstellen, wird ihr Erfolg stark durch die Verletzungsmikroumgebung beeinflusst. Nach Verletzung oder Erkrankung verändert sich die extrazelluläre Matrix (ECM) deutlich
und kann neuronales Überleben und Reparatur einschränken. Diese humane Verletzungsumgebung ist bislang unzureichend verstanden und begrenzt die klinische Umsetzung regenerativer Strategien.
Modelle adulter humaner Hirnverletzungsmikroumgebungen werden durch Dezellularisierung postmortaler Hirngewebeproben verschiedener Pathologien und Altersgruppen etabliert. Die ECM-Zusammensetzung wird hauptsächlich mittels Proteomik charakterisiert. Gesunde Hirn-ECM wird mit pathologiespezifischer ECM verglichen, um alters- und verletzungsbedingte Veränderungen zu identifizieren, die für Regeneration relevant sind. Zwei Reparaturstrategien werden untersucht: die Transplantation humaner iPSC-abgeleiteter Neuronen sowie die Astrozyten-zu-Neuron-Reprogrammierung auf dezellularisierter ECM unter Verwendung junger iPSC-abgeleiteter Astrozyten oder adulter, aus Resektionsmaterial isolierter Astrozyten. Der Einfluss der ECM auf neuronales Überleben, Stressantworten, synaptische Integration und Zellschicksalskonversion wird systematisch analysiert, um das regenerative Potenzial besser zu verstehen und Strategien des neuronalen Ersatzes gezielt zu optimieren.
Das Projekt zielt darauf ab, die extrazelluläre Matrix (ECM) des menschlichen Gehirns zu modellieren, um zu bestimmen, wie die Zusammensetzung der Matrix die neuronale Reparatur beeinflusst. Ersatzstrategien für verlorene Neuronen werden auf dezellularisierter ECM evaluiert, um ECM-Merkmale zu identifizieren, die das Überleben und die Integration von Neuronen regulieren.

Meriam Ernez
Biomedizinisches Zentrum der Ludwig-Maximilians Universität, Institut für Stammzellforschung am Helmholtz Zentrum München & Max-Planck-Institut für Biochemie
Betreut durch

Magdalena Götz
Medizin & BiologieHector Fellow seit 2023