Jenseits der Netzhaut: Maschinelle Lernmodelle zur photochemischen Steuerung von Rhodopsinen
Hector RCD Awardee Prof. Dr. Carolin Müller
Hector Fellow Prof. Dr. Klaus Robert Müller
Hector Fellow Prof. Dr. Peter Hegemann
Das Projekt entwickelt ein maschinelles‑Lern‑Framework, das angeregte‑Zustands‑Eigenschaften von Rhodopsinen präzise vorhersagen kann. Dazu wird ein QM/MM‑Datensatz von Retinal‑Derivaten in proteinähnlichen Umgebungen erzeugt und zum Training einer erweiterten SO3LR‑Modells verwendet. Durch iterative Synthese und ESR‑STM‑ähnliche Spektroskopie von gezielt mutierten Rhodopsin‑Varianten werden die Vorhersagen fortlaufend validiert und optimiert. Die finalen Modelle ermöglichen schnelle, zuverlässige Abschätzungen von Absorptions‑ und Emissionsspektren sowie von Photoreaktionswegen und bilden damit eine daten‑getriebene Plattform für das rationale Design neuer, licht‑responsive Proteine. Beteiligt an diesem Projekt sind Prof. Dr. Carolin Müller, Prof. Dr. Klaus Robert Müller und Prof. Dr. Peter Hegemann.
Rhodopsinen sind lichtempfindliche Proteine, die ein kovalent gebundenes Retinal‑Chromophor als fotoaktive Einheit besitzen. Obwohl alle Rhodopsine diesen gemeinsamen Kern teilen, zeigen sie ein breites Spektrum photochemischer Reaktionen – von einfachen E/Z‑Isomerisationen bis zu mehrstufigen Pfaden – und damit unterschiedliche Funktionen. Diese Vielfalt entsteht aus dem feinen Zusammenspiel zwischen der intrinsischen Reaktivität des Chromophors und der modulierenden Wirkung der umgebenden Proteinmatrix auf den Dunkel‑, den angeregten und den photoproduct‑Zustand. Ein tiefes Verständnis dieser Wechselwirkungen ist Voraussetzung, um die molekularen Prinzipien biologischer Lichtwahrnehmung zu entschlüsseln und die photochemische Reaktivität gezielt zu steuern. Experimentelle Methoden wie zeitaufgelöste UV/Vis‑ und Raman‑Spektroskopie liefern wertvolle Daten, doch die ultrafast‑dynamischen Prozesse erschweren deren Interpretation und führen häufig zu spekulativen Struktur‑Eigenschafts‑Beziehungen. Quantentheoretische Simulationen des angeregten Zustands bieten mechanistische Einblicke, sind jedoch für die großen Chromophor‑Protein‑Komplexe von Rhodopsinen praktisch unzugänglich. Das Vorhaben adressiert diese Limitation, indem ein maschinelles‑Lern‑Framework (ML) entwickelt wird, das angeregte Zustände in kovalent gebundenen Systemen beschreibt und Rhodopsinen als Modell nutzt. Zunächst wird ein hochwertiger QM/MM‑Datensatz von Retinal‑Derivaten in proteinähnlichen Milieus erzeugt, der sowohl Grund‑ als auch angeregte‑Zustands‑Eigenschaften (Geometrien, TD‑DFT‑Energien, Oszillatorstärken, nicht‑adiabatische Kopplungen) beinhaltet. Auf Basis dieses Datensatzes wird das bestehende SO3LR‑Modell erweitert: WP 1 fokussiert die Anpassung von SO3LR zur schnellen und genauen Vorhersage von Grund‑ und Emissionsspektren, indem etwa 100 Rhodopsin‑Strukturen aus dem Protein‑Data‑Bank‑Repository kuratiert und mit hoch‑level QM/MM‑Berechnungen ergänzt werden. WP 2 führt eine fragment‑biasierte Graph‑Neural‑Network‑Kodierung ein, die den retinal‑Fragment gezielt hervorhebt und so die lokalen elektronischen und geometrischen Änderungen, die die angeregten Zustände bestimmen, besser erfasst. WP 3 nutzt die verfeinerten Modelle, um photochemische Reaktionspfade zu prognostizieren; dazu werden interpolierte Geometrien zwischen relevanten Minima, konstruierte Konikalen Schnittpunkte und CASPT2‑optimierte Potentialflächen generiert, und das trainierte Netzwerk liefert Energien, Kräfte und approximative nicht‑adiabatische Kopplungen für S₀‑ und S₁‑Zustände, die in Surface‑Hopping‑Dynamiken (z. B. SHARC) eingesetzt werden. WP 4 schließt den iterativen Lern‑Loop: Model‑vorgeschlagene Varianten (z. B. rot‑verschobene Absorption oder hohe Fluoreszenz‑Quantenausbeute) werden in Pichia pastoris oder HEK‑Zellen exprimiert, mittels affinitätsbasierter Reinigung isoliert und durch statische sowie zeitaufgelöste Raman‑, UV/Vis‑ und FTIR‑Spektroskopie charakterisiert; femtosekunden‑Raman‑Messungen erfolgen in Zusammenarbeit mit externen Partnern. Die experimentellen Ergebnisse fließen zurück in die Modelloptimierung. Das Projekt vereint die Kompetenzen von Prof. Dr. Klaus Robert Müller (Maschinelles Lernen für Chemie und Physik), Prof. Dr. Carolin Müller (hochwertige QM/MM‑Daten und Erweiterung von ML‑Modellen für angeregte Zustände) und Prof. Dr. Peter Hegemann (synthetische, exprimierte und spektroskopisch untersuchte Rhodopsin‑Derivate). Durch die Kombination von massenselektiver Ion‑Soft‑Landing und ESR‑STM entsteht ein noch nicht vorhandener methodischer Durchbruch, der eine modulare Plattform für den kontrollierten Aufbau beliebiger molekularer Bausteine und deren Spin‑Kopplung bereitstellt und sich nahtlos auf größere Biomoleküle (z. B. Metall‑Proteine) übertragen lässt. Langfristig wird ein offenes Werkzeug‑Set für die Gemeinschaft geschaffen, das elementare Oberflächenphysik mit Quanten‑Information und Sensorik verknüpft und die Basis für die nächste Generation molekularer Quantensimulatoren und optogenetischer Werkzeuge legt.
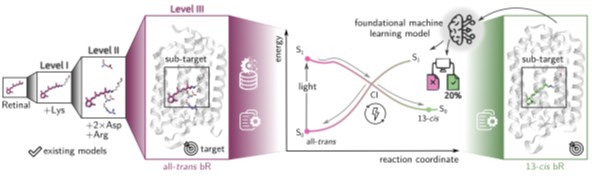
Abbildung 2: Illustration des übergeordneten Projektziels: Entwicklung von Machine‑Learning‑Modellen für angeregte Zustände, um über Retinal‑Modellsysteme (links) hinauszugehen und fotoinduzierte Phänomene des Retinals in seiner nativen Protein‑Umgebung (farbige Kästchen) vorherzusagen. Dies wird durch die Kombination von computergestützter Chemie, Machine Learning und Spektroskopie zur Etablierung eines grundlegenden ML‑Frameworks angegangen.
Betreut durch

Carolin Müller
Chemie, Informatik

Klaus-Robert Müller
Informatik, Mathematik & PhysikHector Fellow seit 2023

Peter Hegemann
Biologie, Chemie & MedizinHector Fellow seit 2015